CO-ORDINATE (DATIVE COVALENT) BONDING
عبارة عن رابطة تساهمية تساهم فيها إحدى الذرتين بالزوج الالكتروني الرابط بينما يقتصر دور الذرة الأخرى على المساهمة بمجال فارغ .
مثال1 : في تفاعل النشادر مع كلوريد الهيدروجين لانتاج ملح كلوريد الأمونيوم تتكون رابطة تناسقية بين ذرة النيتروجين في النشادر وذرة الهيدروجين في كلوريد الهيدروجين .
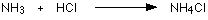
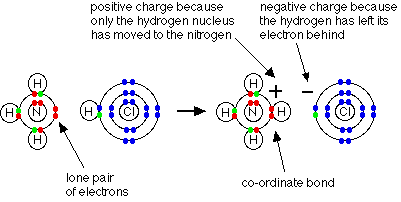
فالرابطة التناسقية تتكون بين ( ذرة مانحة ) تتكون عليها شحنة موجبة و ( ذرة مستقبلة ) تتكون عليها شحنة سالبة ويشار إلى الرابطة التناسقية عادةً بسهم يتجه من الذرة المانحة إلى الذرة المستقبلة .
وحقيقة ما حدث في التفاعل السابق هو ارتباط جزيء النشادر بالبروتون ليتكون أيون الأمونيوم .

مثال2 : عند إذابة غاز كلوريد الهيدروجين في الماء لتكوين حمض الكلور تتكون رابطة تناسقية بين ذرة الأكسجين في الماء وذرة الهيدروجين في كلوريد الهيدروجين .


وهنا تكون ذرة الأكسجين هي الذرة المانحة وذرة الهيدروجين الذرة المستقبلة .
مثال 3 : في تفاعل النشادر مع ثالث فلوريد البورون تتكون رابطة تناسقية بين ذرة النيتروجين ( المانحة ) وذرة البورون ( المستقبلة ).



وتسمى المركبات الحاوية للراوبط التناسقية بالمركبات التناسقية ، والجدير بالذكر أن معظم العناصر الانتقالية ترتبط بروابط تناسقية وتكوّن هذا النوع من المركبات .
الرابطة الهيدروجينية
عبارة عن تجاذب كهربي ضعيف بين جزيئات المركب التساهمي القطبي المحتوي على ذرة هيدروجين .
مثال : الرابطة الهيدروجينية في الماء

وكما يتضح من المثال فإن الرابطة الهيدروجينية تربط الجزء السالب ( ذرة ذات سالبية كهربية عالية ) في جزيء المادة بالطرف الموجب ( ذرة هيدروجين ) في جزيء أخر .
أثر الرابطة الهيدروجينية على خواص المادة
تؤثر الروابط الهيدروجينية على الخواص الطبيعية للمادة ، فدرجات غليان وانصهار المواد المحتوية على روابط هيدروجينية أعلى من درجات غليان وانصهار مثيلاتها من المواد ويبرز هذا الأثر بشكلٍ واضح في خواص الماء ،فللماء صفات خاصة ترجع إلى الروابط الهيدروجينية المميزة التي تربط بين جزيئاته ، فدرجة غليان الماء ( 100 درجة م ) مرتفعة جداً إذا ما قورنت بدرجات غليان مركبات عناصر المجموعة السادسة مع الهيدروجين بالرغم من أن الوزن الجزيء للماء أقل من الوزن الجزيء لهذه المركبات .
كما أن للروابط الهيدروجينية التي تربط بين جزيئات الماء تأثير مباشر في القيمة العليا للكثافة التي يتخذها الماء والتي تساوي 1 جم / سم مكعب عند 4 درجة مئوي بينما تكون كثافة الماء أقل من ( 1جم/سم مكعب ) عند أعلى وأقل من ( 4 درجة م ) وهذا ما يجعل الجليد يطفوا على سطح التجمعات المائية عند تجمد الماء .
وأيضاً ترجع خاصية التوتر السطحي المميزة في الماء إلى ارتباط جزيئات الماء بروابط هيدروجينية .
وفيما يلي مقارنة بين الماء والميثان من حيث درجة الغليان ودرجة الانصهار :
Relative molecular mass
Melting point /°C
Boiling point /°C
CH4
16 Relative molecular mass
-182 Melting point /°C
-164 Boiling point /°C
H2O
18 Relative molecular mass
0 Melting point /°C
100 Boiling point /°C
يلاحظ الفرق الكبير في درجة الغليان والانصهار بين المركبين فالماء درجة غليانه وانصهاره أعلى بكثير من درجة غليان وانصهار الميثان بالرغم من تقارب الوزن الجزيئي لهما . وبالطبع فإن السبب يرجع إلى قوة الروابط الهيدروجينية الموجودة في الماء .
الرابطة الفلزية ( METALLIC BONDING )
جميع الفلزات ( ماعدا الزئبق ) توجد في الحالة العنصرية في الحالة الصلبة ولعل سبب ذلك هو تلك الروابط القوية التي تربط بين ذرات الفلز ( المعدن ) فيمكن النظر إلى الفلز في الحالة الصلبة كبحرٍ من الشحنات الموجبة ( الأنوية ) تتحرك بينها الالكترونات بحرية وتنتقل من ذرة إلى أخرى .
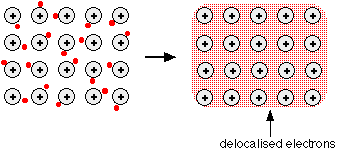
وترجع الكثير من خصائص الفلزات الطبيعية إلى طبيعة هذه الرابطة فالتوصيل الكهربي والتوصيل الحراري للفلزات سببه هو حركة الالكترونات الحرة بين الذرات .

روابط ( قوى ) فان درفال
ترتبط جزيئات المركبات التساهمية غير القطبية بعضها ببعض بروابط فيزيائية ضعيفة جداً ناتجة من تجاذب أنوية الذرات في جزيء معين مع الكترونات التكافؤ في جزيء مجاور ، يطلق على هذه القوى روابط فان درفال .
ومثال ذلك ترتبط جزيئات الهالوجينات في حالتها العنصرية بروابط فان درفال ونجد أنه بنزولنا إلى أسفل في المجموعة ( من الفلور إلى اليود ) تزداد قوة روابط فان درفال بسبب ازدياد العدد الذري ( عدد البروتونات في الأنوية وعدد الالكترونات في مستويات الطاقة الالكترونية ) لذلك نجد أنه كلما نزلنا إلى أسفل في المجموعة تزداد كثافة الهالوجين كما تزداد درجة غليانه وانصهاره . ( الحقيقة هناك عامل أخر يسبب هذه الزيادة وهو ازدياد الوزن الجزيئي بنزولنا إلى أسفل في مجموعة الهالوجينات ) فبينما نجد الفلور غاز خفيف نجد الكلور غاز أثقل منه والبروم سائل واليود مادة صلبة .
عبارة عن رابطة تساهمية تساهم فيها إحدى الذرتين بالزوج الالكتروني الرابط بينما يقتصر دور الذرة الأخرى على المساهمة بمجال فارغ .
مثال1 : في تفاعل النشادر مع كلوريد الهيدروجين لانتاج ملح كلوريد الأمونيوم تتكون رابطة تناسقية بين ذرة النيتروجين في النشادر وذرة الهيدروجين في كلوريد الهيدروجين .
فالرابطة التناسقية تتكون بين ( ذرة مانحة ) تتكون عليها شحنة موجبة و ( ذرة مستقبلة ) تتكون عليها شحنة سالبة ويشار إلى الرابطة التناسقية عادةً بسهم يتجه من الذرة المانحة إلى الذرة المستقبلة .
وحقيقة ما حدث في التفاعل السابق هو ارتباط جزيء النشادر بالبروتون ليتكون أيون الأمونيوم .

مثال2 : عند إذابة غاز كلوريد الهيدروجين في الماء لتكوين حمض الكلور تتكون رابطة تناسقية بين ذرة الأكسجين في الماء وذرة الهيدروجين في كلوريد الهيدروجين .
وهنا تكون ذرة الأكسجين هي الذرة المانحة وذرة الهيدروجين الذرة المستقبلة .
مثال 3 : في تفاعل النشادر مع ثالث فلوريد البورون تتكون رابطة تناسقية بين ذرة النيتروجين ( المانحة ) وذرة البورون ( المستقبلة ).

وتسمى المركبات الحاوية للراوبط التناسقية بالمركبات التناسقية ، والجدير بالذكر أن معظم العناصر الانتقالية ترتبط بروابط تناسقية وتكوّن هذا النوع من المركبات .
الرابطة الهيدروجينية
عبارة عن تجاذب كهربي ضعيف بين جزيئات المركب التساهمي القطبي المحتوي على ذرة هيدروجين .
مثال : الرابطة الهيدروجينية في الماء

وكما يتضح من المثال فإن الرابطة الهيدروجينية تربط الجزء السالب ( ذرة ذات سالبية كهربية عالية ) في جزيء المادة بالطرف الموجب ( ذرة هيدروجين ) في جزيء أخر .
أثر الرابطة الهيدروجينية على خواص المادة
تؤثر الروابط الهيدروجينية على الخواص الطبيعية للمادة ، فدرجات غليان وانصهار المواد المحتوية على روابط هيدروجينية أعلى من درجات غليان وانصهار مثيلاتها من المواد ويبرز هذا الأثر بشكلٍ واضح في خواص الماء ،فللماء صفات خاصة ترجع إلى الروابط الهيدروجينية المميزة التي تربط بين جزيئاته ، فدرجة غليان الماء ( 100 درجة م ) مرتفعة جداً إذا ما قورنت بدرجات غليان مركبات عناصر المجموعة السادسة مع الهيدروجين بالرغم من أن الوزن الجزيء للماء أقل من الوزن الجزيء لهذه المركبات .
كما أن للروابط الهيدروجينية التي تربط بين جزيئات الماء تأثير مباشر في القيمة العليا للكثافة التي يتخذها الماء والتي تساوي 1 جم / سم مكعب عند 4 درجة مئوي بينما تكون كثافة الماء أقل من ( 1جم/سم مكعب ) عند أعلى وأقل من ( 4 درجة م ) وهذا ما يجعل الجليد يطفوا على سطح التجمعات المائية عند تجمد الماء .
وأيضاً ترجع خاصية التوتر السطحي المميزة في الماء إلى ارتباط جزيئات الماء بروابط هيدروجينية .
وفيما يلي مقارنة بين الماء والميثان من حيث درجة الغليان ودرجة الانصهار :
Relative molecular mass
Melting point /°C
Boiling point /°C
CH4
16 Relative molecular mass
-182 Melting point /°C
-164 Boiling point /°C
H2O
18 Relative molecular mass
0 Melting point /°C
100 Boiling point /°C
يلاحظ الفرق الكبير في درجة الغليان والانصهار بين المركبين فالماء درجة غليانه وانصهاره أعلى بكثير من درجة غليان وانصهار الميثان بالرغم من تقارب الوزن الجزيئي لهما . وبالطبع فإن السبب يرجع إلى قوة الروابط الهيدروجينية الموجودة في الماء .
الرابطة الفلزية ( METALLIC BONDING )
جميع الفلزات ( ماعدا الزئبق ) توجد في الحالة العنصرية في الحالة الصلبة ولعل سبب ذلك هو تلك الروابط القوية التي تربط بين ذرات الفلز ( المعدن ) فيمكن النظر إلى الفلز في الحالة الصلبة كبحرٍ من الشحنات الموجبة ( الأنوية ) تتحرك بينها الالكترونات بحرية وتنتقل من ذرة إلى أخرى .
وترجع الكثير من خصائص الفلزات الطبيعية إلى طبيعة هذه الرابطة فالتوصيل الكهربي والتوصيل الحراري للفلزات سببه هو حركة الالكترونات الحرة بين الذرات .

روابط ( قوى ) فان درفال
ترتبط جزيئات المركبات التساهمية غير القطبية بعضها ببعض بروابط فيزيائية ضعيفة جداً ناتجة من تجاذب أنوية الذرات في جزيء معين مع الكترونات التكافؤ في جزيء مجاور ، يطلق على هذه القوى روابط فان درفال .
ومثال ذلك ترتبط جزيئات الهالوجينات في حالتها العنصرية بروابط فان درفال ونجد أنه بنزولنا إلى أسفل في المجموعة ( من الفلور إلى اليود ) تزداد قوة روابط فان درفال بسبب ازدياد العدد الذري ( عدد البروتونات في الأنوية وعدد الالكترونات في مستويات الطاقة الالكترونية ) لذلك نجد أنه كلما نزلنا إلى أسفل في المجموعة تزداد كثافة الهالوجين كما تزداد درجة غليانه وانصهاره . ( الحقيقة هناك عامل أخر يسبب هذه الزيادة وهو ازدياد الوزن الجزيئي بنزولنا إلى أسفل في مجموعة الهالوجينات ) فبينما نجد الفلور غاز خفيف نجد الكلور غاز أثقل منه والبروم سائل واليود مادة صلبة .
