ينشر «مدرس اون لاين» ملخص قوانين مادة الكيمياء للصف الثالث الثانوي, في 8 ورقات لكل المنهج وهي مهمة جدا لكل الطلاب ..
اذا كانت العلاقة بين kc و درجة الحرارة علاقة طردية كان التفاعل ماص للحرارة
اذا كانت العلاقة بين Kc و درجة الحرارة علاقة عكسية كان التفاعل طارد للحرارة
القيمة الصغيرة لثابت الإتزان ( أقل من الواحد الصحيح )
أن الضغوط الجزيئية للمتفاعلات أكبر من الضغوط الجزيئية للنواتج
و هذا يعنى أن التفاعل العكسى هو السائد
القيمة الكبيرة لثابت الإتزان
تعنى أن الضغوط الجزيئية للنواتج أكبر من الضغوط الجزيئية للمتفاعلات
وأن التفاعل يستمر قرب نهايتهاى أن التفاعل الطردي هو السائد...
تابع كل قوانين مادة الكيمياء كاملة ٣ ثانوي

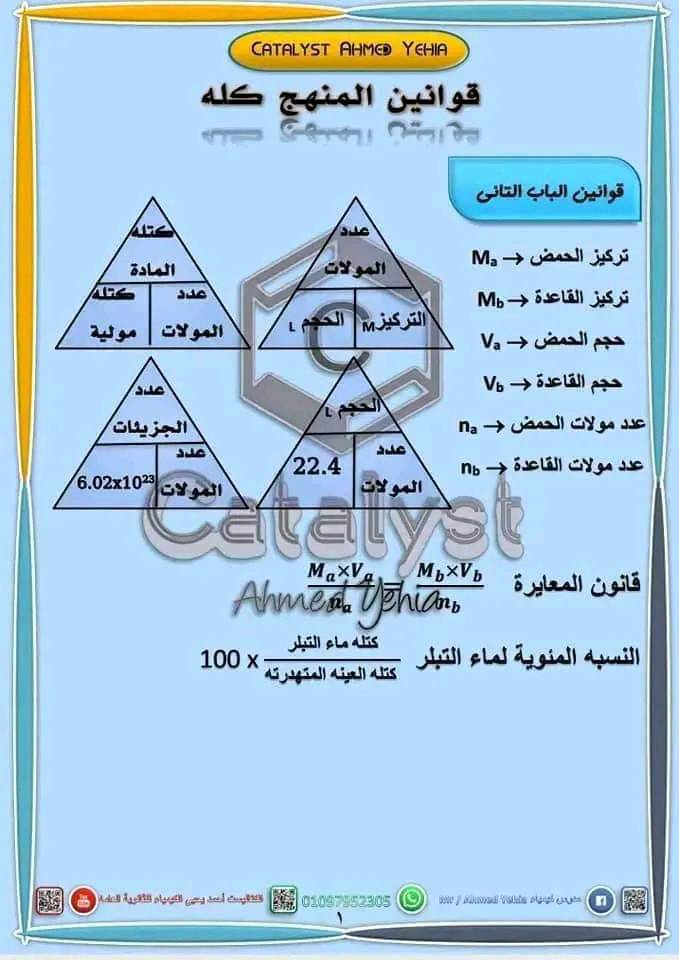



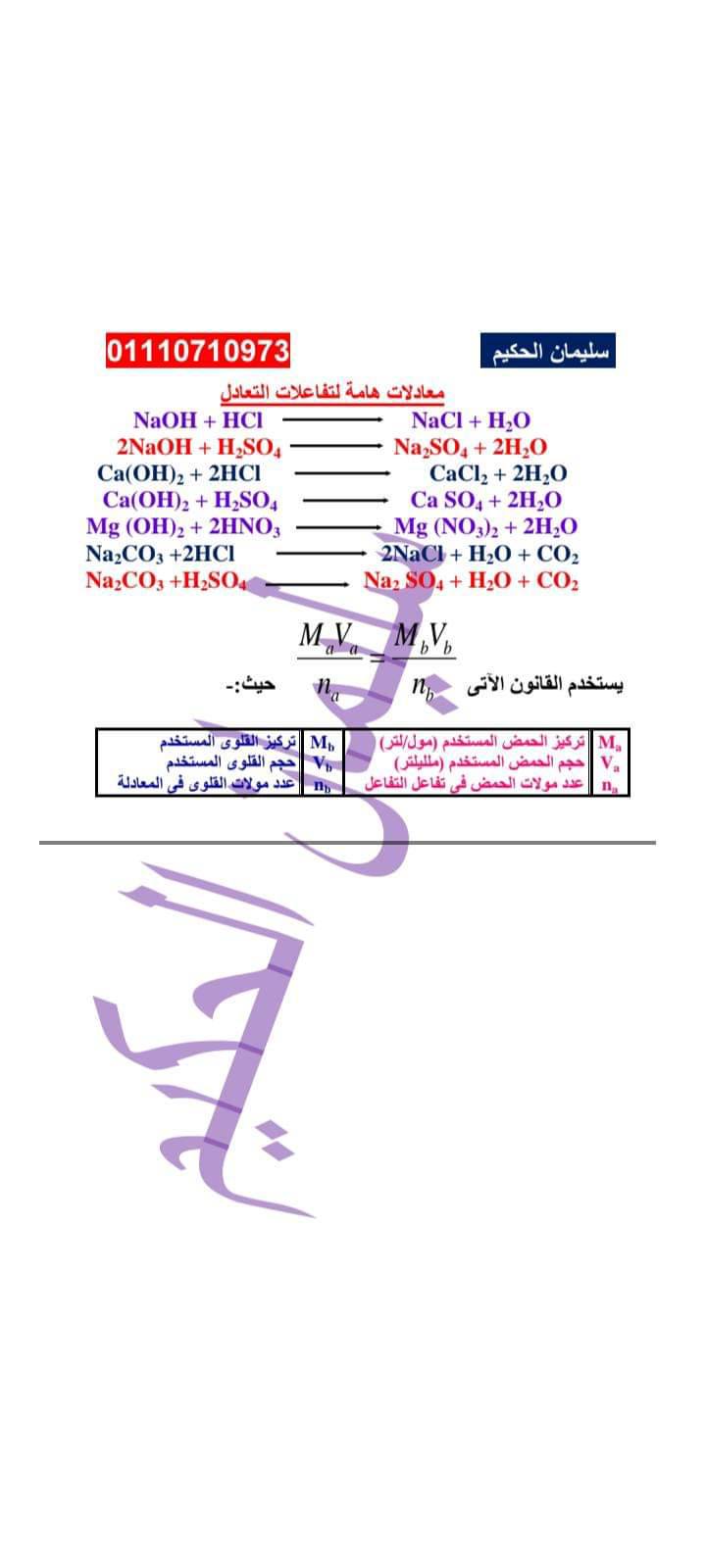



عندما يحدث تفاعل كيميائي بين مركبين، يتم قياس كمية كل مركب في وحدة معينة، مثل الجرامات أو الأونصات. ولكن بالنسبة للتفاعلات الكيميائية، ليس من الأمر المهم معرفة كمية كل مركب بحد ذاته، بل كمية المركبات المتفاعلة التي تشارك في التفاعل.
لذلك، يتم استخدام المولات المتفاعلة كوحدة قياس لكمية المواد المشاركة في التفاعل الكيميائي. وتشير المول إلى عدد الذرات أو الجزيئات الموجودة في مول واحد من المادة.
وبشكل عام، يمكن تحويل كمية المادة من الوحدات الأخرى إلى المولات المتفاعلة باستخدام الصيغة التالية:
عدد المولات = الكمية / الوزن المولي
حيث الكمية تشير إلى كمية المادة المقاسة بالوحدة المختارة، والوزن المولي هو كتلة مول واحد من المادة المذكورة، ويتم تحديدها بوحدة الغرام/المول.
Professor2023-06-22, 8:34 pm